斯微生物mRNA技术,演化新一代医学革命
2022-07-13 10:23:11 来源: 壹点网
文章源自公众号:弗若斯特沙利文
随着我国医疗水平的不断提高,国内大部分医药科技公司获得了卓越的成就,上海斯微生物就是mRNA疫苗研发的佼佼者,上海斯微生物不断的攻克难关,不怕困难,勇往直前,这种精神就值得我们学习。
1、mRNA技术概览
基于mRNA技术的疗法,是将体外合成的mRNA递送到人体中的特定细胞,mRNA在细胞质中被翻译成所需的蛋白质。mRNA作为疫苗或药物,可应用于预防传染病、治疗肿瘤和蛋白替代疗法。
l 传染病领域预防性疫苗
针对传染性疾病的mRNA疫苗编码相关病原体的抗原,注射后可在体内表达出特异性的抗原,可同时诱导细胞免疫和体液免疫,刺激产生相应抗体和免疫细胞,用以预防相应病原体。
l 肿瘤治疗性疫苗
将编码肿瘤特异性抗原靶点的mRNA通过特定的方式递送到体内,使这些肿瘤特异性抗原翻译并呈递到细胞表面,进而激活免疫系统,使其能特异性识别并杀伤肿瘤细胞。
l 蛋白替代疗法
通常情况下,蛋白质替代疗法用于治疗罕见的单基因疾病,旨在恢复酶的功能。蛋白质合成困难,给药存在诸多难题且价格昂贵,而利用mRNA将人体变成自身蛋白质的加工厂,理论上是经济可行且高效的方式。mRNA药物靶点丰富,不受靶点蛋白成药性,胞内/外限制。mRNA序列设计简便,利用患者自身细胞产生分子,绕过化学合成中的挑战,且自身诱导产生的分子药效更强。mRNA生产平台具有较强的延展性和可复制性,易于规模化生产。
2、mRNA市场分析及竞争格局
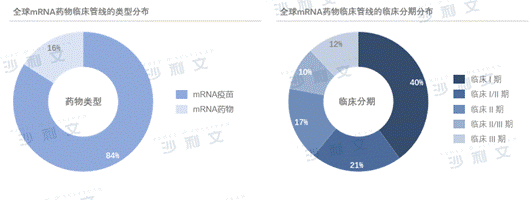
在全球,mRNA技术已成为各大药企和生物技术公司积极布局的重要赛道。以Moderna、BioNTech和CureVac为代表的国际企业,除了在传染病领域布局多种预防性疫苗,还在肿瘤治疗领域进行相关布局,包括通用型肿瘤疫苗、个性化肿瘤疫苗和肿瘤细胞因子补充。据统计,截至2022年3月31日,全球mRNA药物进入临床管线的共有56个,研发主要集中在疫苗领域,约占84%,而治疗性药物占比约为16%。除mRNA新冠疫苗紧急上市外,其他大多处于早期阶段,mRNA研发主要处于临床I期阶段,约占总数量的40%。
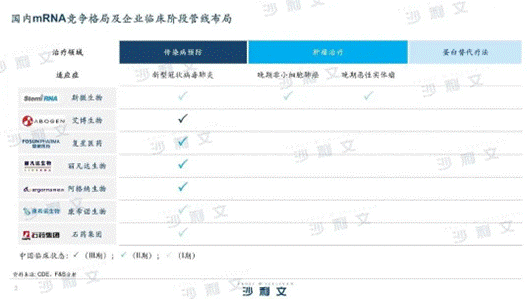
在国内,mRNA市场仍处于早期发展阶段,已有数家生物技术公司在研发上展现出潜力,7家公司的mRNA药物获得CDE临床批件,其中上海斯微生物是拥有临床阶段管线最多,且涉及适应症最广的公司。上海斯微生物管线聚焦于传染病预防和肿瘤治疗两大领域,新冠mRNA疫苗产品正在全球开展II期临床试验,在国内开展I期临床试验,针对晚期实体瘤(包括肺癌、食管癌和消化道肿瘤)的个性化肿瘤疫苗产品正在全球和中国开展临床I期试验。
2020年底,由Pfizer/BioNTech和Moderna分别研发的两款mRNA新冠疫苗获得紧急使用授权,2021年两款疫苗全球销售额高达587亿美元。与传统疫苗相比,mRNA疫苗研制周期短,序列易于修改,能够快速更新迭代以响应不断出现的变异毒株,生产基于通用的技术平台,提供了灵活的、大规模的、快速的、具有成本效益的生产流程,且产能爬坡速度极快,批次产量可以达到亿剂, 应对突发性流行病学危机优势明显;mRNA疫苗打破了传统灭活、减毒活疫苗的免疫激活模式,创新性利用人体本身细胞表达抗原蛋白,可以诱导更为广泛有效的细胞免疫及体液免疫反应,产生更高的保护率。同时,相较于其他创新性疫苗(如DNA疫苗,毒性较强且需要进入细胞核中转录为mRNA,而mRNA只需要进入细胞质就能表达)具有更高的安全性,数亿剂mRNA新冠疫苗的接种,其安全性得到了充分的验证。mRNA技术优势明显,将会是新型疫苗开发的首要选择。
短期而言,预防性疫苗市场主要源于新冠产品,中长期而言,凭借mRNA疫苗在靶点数量、疗效、安全性和生产工艺的优势,会拓展到更多感染性疾病的预防中,如流感病毒疫苗、流感呼吸道合胞病毒疫苗、疟疾疫苗等领域。除预防性疫苗外,免疫疗法治疗肿瘤也是目前mRNA技术的研究热点,传统的免疫疗法需注射抗原到体内,蛋白质给药存在诸多困难,合成困难且价格昂贵,而注射人工合成的mRNA到体内,指导人体合成对应的抗原蛋白,是有效且经济的方式。在肿瘤治疗领域,存在大量的患者数量及临床未满足需求,未来肿瘤治疗性疫苗市场规模会持续攀升。总体而言,在递送技术和稳定性方面取得改善和进步以后,mRNA具有非常强的竞争优势,有潜力成为跨应用领域的产品,市场发展空间广阔。
3、mRNA疗法核心技术及挑战——药物递送系统
由于mRNA分子量大、免疫原性强、容易降解,需借助递送系统以发挥作用。递送系统与mRNA分子结合,需在全身给药时保护其不被血清中的RNA水解酶降解,从而保证mRNA可以顺利到达靶细胞,然后以内涵体通过胞吞作用进入细胞。通常情况下,内涵体进入细胞质后,会被直接送至溶酶体进行分解。因此,递送系统还需在内涵体到达溶酶体前,将mRNA从内涵体中释放出来。mRNA逃离内涵体进入细胞质后,会游动至核糖体并在此翻译为蛋白质。
mRNA疫苗常用的递送方法和载体
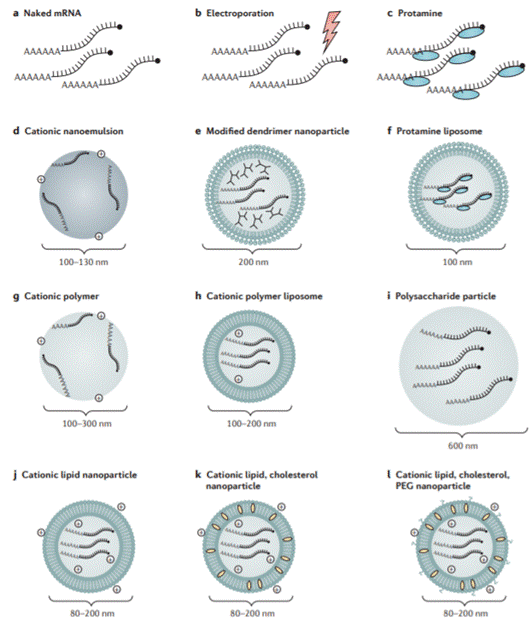
mRNA主流的递送系统从鱼精蛋白逐步发展脂质类递送系统。脂质类递送系统包括脂质体(liposome)、脂质纳米粒(lipid Nanoparticle,LNP)、脂质多聚物纳米载体(Lipopolyplex,LPP)。脂质类中的LPP是一种以聚合物包载mRNA为内核、磷脂包裹为外壳的双层结构。LPP的双层脂质体膜具有更好的包载、保护mRNA的效果,LPP的内核能够随聚合物的降解逐步释放mRNA分子。LPP靶向树突状细胞效果优异,能够更好的通过抗原递呈激活T细胞的免疫反应,达到理想的治疗效果。斯微生物是唯一一家使用非LNP递送系统的公司,并拥有LPP自主知识产权。

4、mRNA技术应用前景及未来趋势
mRNA技术在新冠疫苗研发中大放异彩,有望拓展到肿瘤治疗、再生医学等更广阔的治疗领域。肿瘤治疗领域中,存在大量的患者数量及临床未满足需求。相对其他技术而言,mRNA在肿瘤疫苗尤其是个性化疫苗方面具有一定的优势。mRNA易于同时表达20个以上的肿瘤抗原,序列设计和生产快速,是最具个性化肿瘤疫苗潜力的技术平台。
个性化治疗性肿瘤疫苗,通过测序,确定患者肿瘤细胞独有新抗原,利用mRNA针对新生抗原开发各种个性化肿瘤疫苗。BioNTech和Moderna相应的管线已走向临床。在国内,上海斯微生物是目前唯一拥有临床阶段mRNA个性化肿瘤疫苗的公司,相应的管线已进入临床I期阶段。再生医学领域中,通过mRNA可向纤维细胞转染编码重编程因子产生IPS细胞,诱导分化成功能细胞,例如上海斯微生物通过向纤维细胞转染编码重编程因子(Oct4、Sox2、c-Myc、Klf4)的mRNA,产生iPS细胞,诱导其向心肌细胞分化,致力于通过mRNA诱导干细胞治疗心血管疾病。
以上就是上海斯微生物对mRNA疫苗研发的浅解,也凸显出上海斯微生物对mRNA疫苗研发的决心,加油上海,加油斯微生物!
免责声明:市场有风险,选择需谨慎!此文仅供参考,不作买卖依据。
标签:
为您推荐
精彩放送
热门文章
-

精彩看点:国家统计局:11月份CPI同比上涨1.6% 环比下降0.2%
-

世界微速讯:国家统计局:11月猪肉价格由涨转降 环比下降0.7%
-

【全球速看料】三大应用领域齐头并进 数字人民币场景持续扩容
-

创新产品不断落地 熊猫债市场扩容有潜力
-

世界报道:新亚制程:拟7亿元收购杉杉新材料51%股权
-

环球短讯!沃森生物:公司新冠mRNA疫苗的国内III期临床试验数据整理及统计分析工作已进入尾声
-

今日最新!南财研选快讯丨中信建投:持续看好白酒、啤酒、调味品、餐饮等板块明年的修复机会
-

【环球新视野】拓新药业:捐赠278.1万元用于采购国产新冠口服药阿兹夫定片
-

全球时讯:益生股份:11月白羽肉鸡苗销售收入2.43亿元
-

焦点观察:国家卫健委发布关于进一步优化发热患者就诊流程的通知
-

【天天速看料】鞍重股份:拟与联合体260亿元投建碳酸锂等项目
-

环球热门:正邦科技:11月生猪销售收入5.14亿元 环比降26.22%
精彩图片
-

成本大减!新一轮的旗舰大战也将在即将到来的9月正式拉开帷幕
-

博览会开幕 中国首款具有自主知识产权的国产通用型科学计算软件正式发布
-

技术下降!Intel独立显卡驱动一次评测就发现43个Bug
-

高性能的台式机彻底告别“光污染” 雷克沙推出简洁纯白外观设计
-

韩国媒体率先报道:三星电子236层NAND闪存预计年内开始生产 市场竞争更激烈
-

新科技!苹果正在积极研发某种形式的AR/VR头显或智能眼镜
-

谷歌测试开展新功能 向用户展示哪些云流媒体服务拥有特定的视频游戏
-

支付宝积极响应国家为小微降费的政策号召 一年降费让利近80亿
-

京东汽车就与浦林成山旗下新能源车轮胎品牌浦林达成战略合作 助力轮胎“电动化转型”
-

苹果新专利公布:暗示未来 iPhone手机或许有陶瓷材质版
-

盖茨和韩国能源供应商SK共同牵头 其中SK投资2.5亿美元
-

海底捞早已经捞不动了 据统计上半年最高亏损达2.97亿
热文
-

央行、外汇局:进一步规范境外机构境内发行债券资金管理
-

天天新消息丨《阿凡达2:水之道》预售总票房破4000万 首日排片超10万场
-

当前最新:湖北设立5亿元中小微企业应急转贷纾困基金
-

火星冲日与火星伴月今晚将同时上演
-

天天快资讯丨多家上市公司生产线暂停 “亚洲锂都”宜春为何陷环保风波?
-

天天热门:广东消委会发布“农村电商消费”调查报告
-

世界头条:新冠是否应回归乙类管理?张伯礼:条件日趋成熟 适时有序调整
-

全球最新:融资最新持仓曝光!加仓医药生物、休闲服务、采掘
-

杭银消金发行10亿元ABS 客户征信维护难题待解
-

环球微动态丨中资地产美元债一二级市场仍有“温差” 明年二季度发行或迎改善
-

当前关注:业内人士:未来银行理财产品有望在产品类型、投资者门槛和市场培育上进一步完善
-

防疫政策调整后 多地核酸采样、核酸检测采购项目宣告终止
-

美国第三季度非农企业部门劳动生产率增长0.8%
-

两市融资余额增加26.84亿元
-

人民银行山西五台县支行 打好金融支持“三张牌” 助推特色产业发展
-

发展露营旅游 对农村金融机构意味着什么
-

焦点快播:新冠终结者来了?这股突然暴涨!更有AI造就国产App海外火了
-

全球百事通!今年前11个月我国进出口同比增长8.6% 民营企业进出口快速增长
-

当前时讯:大商所大宗商品仓单登记中心即将上线
-

热推荐:宁德时代:2022年累计新增借款392.07亿元
-

净值多次“跳水”再拉升,年化波动率超15%,混合理财为何“混”而不“清”?丨机警理财日报(12月7日)
-

每日关注!上海市进一步优化调整相关疫情防控措施
-

世界即时看!华纳药厂:子公司原料药右布洛芬获得上市申请批准通知书
-

环球头条:舆情预警丨南投集团:企业子公司部分股权无偿划转
-

每日讯息!江苏阳光:终止内蒙古对外投资事项 将拟投资的光伏项目的项目地选在宁夏石嘴山
-

A股共113只个股发生大宗交易 总成交46.64亿元
-

全球速读:九典制药:公司有生产销售化学原料药熊去氧胆酸
-

解密主力资金出逃股 连续5日净流出407股
-

环球微速讯:广汇能源:白石湖露天煤矿产能核增至1800万吨/年获批
-

山鹰国际:参与设立投资基金并向子公司增资
-

当前要闻:广宇发展:获取陕西、内蒙古新能源项目建设指标
-

世界观热点:前十一月新能源产品出口增长迅速 世界杯热潮下足球经济成热点
-

涨跌幅是什么意思?什么因素影响着股票的跌涨?
-

怎么可以全部提取公积金?公积金贷款后还需要缴纳公积金吗?
-

全球热推荐:旭辉控股集团:1-11月累计合同销售1175.9亿元
-

环球要闻:隆基绿能:拟30亿元芜湖投建年产15GW单晶组件项目
-

焦点!重庆银保监局出台16条措施支持复工复产
-

世界聚焦:四部门:实施涉农专业人才培养“入学有编、毕业有岗”改革试点
-

天天快看点丨龙虎榜丨安奈儿今日涨停,上榜营业部席位全天成交1.94亿元
-

新包装上市!Meco蜜谷果汁茶去标签更环保
-

环球短讯!上海:进一步降低制度性交易成本更大激发市场主体活力
-

世界资讯:华秦科技:拟与光声超构投资设立合资公司
-

环球热资讯!我国防疫策略调整是否晚于其他国家?国家卫健委回应
-

天天微资讯!舆情预警丨宣泰医药:熊去氧胆酸能否用于新冠病毒预防及感染的治疗仍存在重大不确定性
-

全球资讯:天山股份:拟与冀东水泥共设合资公司
-

全球今亮点!中国11月外汇储备规模为31175亿美元
-

世界速看:“代理退保”黑产花样多 江西、安徽等多地征集犯罪线索 消费者该如何识别?
-

国家卫健委:已要求医疗机构及药品零售网点加强药物储备,没有必要去囤积和抢购药物
-

消息!泰国11月CPI同比上涨5.55%,低于预期
-

全球微速讯:A股收评:指数午后冲高回落 熊去氧胆酸概念股领涨












